Cómo reconvertir el CO2 en carbono
Un grupo de investigadores australianos ha desarrollado un método para reconvertir el CO2 en carbono. Transformar el dióxido de carbono (CO2) en un material sólido similar el carbono es un avance podría revolucionar el enfoque mundial sobre captura y almacenamiento de este gas de efecto invernadero.
En un estudio publicado en detalle en Nature Communications, el investigador Torben Daeneke de la Universidad RMIT de Melbourne, aclara que “gracias a los metales líquidos que hemos utilizado como catalizadores, demostramos que también es posible lograrlo a temperatura ambiente, en un proceso que es a la vez eficiente y escalable”.
Características del estudio
Las primeras investigaciones giraron alrededor de la posibilidad de capturar y de almacenar el carbono y condensarlo en una forma líquida. El objetivo final es transportarlo e inyectarlo bajo tierra o utilizarlo para producir combustibles.
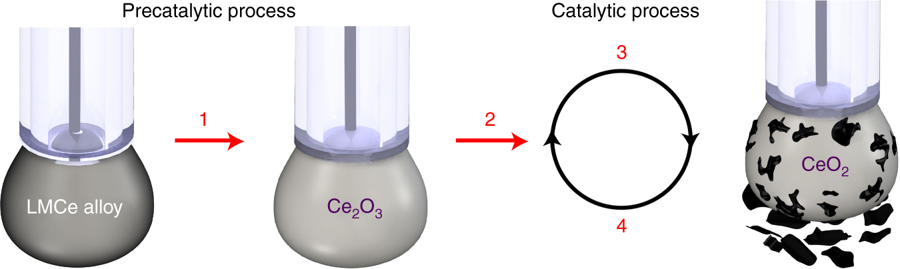
Ahora, para reconvertir el CO2 en carbono han diseñado un catalizador a partir de una aleación de galio no tóxico. Un catalizador que activa el proceso y lo hace eficaz a la hora de conducir señales eléctricas. Así, el CO2 se disuelve en un recipiente con líquido electrolítico y una leve cantidad de metal. Después, carga la mezcla con una corriente eléctrica. De esta manera, el CO2 se deposita en escamas sólidas de carbono, un estado en el que es mucho más fácil almacenarlo.
Cómo reconvertir el CO2 en carbono
El CO2 es una molécula notablemente estable. Por lo tanto, el diseño de electrocatalizadores de reducción de CO2 que funcionan a bajo sobrepotencial y a temperatura ambiente es un desafío. Se han seguido dos enfoques dominantes hasta la fecha. El primero es que el CO2 se reduce en su forma gaseosa a alta temperatura. En el segundo, el CO2 disuelto se reduce electrocatalíticamente en un entorno líquido. La ruta gaseosa se basa típicamente en catalizadores de óxido que pueden reducir el CO2 a CO a altas temperaturas. Alternativamente, la electroquímica líquida basada en electrolitos se puede utilizar para producir una gama de moléculas pequeñas que incluyen CO, C2H4, CH4, HCO2H y CH3OH6.
Estas moléculas son de importancia comercial para las industrias químicas. Aun así, no son adecuadas cuando el objetivo principal es la eliminación indefinida de CO2 de la atmósfera en la escala Gt. Las moléculas también son contaminantes volátiles y potentes.
La reducción de CO2 a productos sólidos es un desafío. Cualquier producto puede cubrir la superficie del catalizador a través de la adhesión de van der Waals, bloqueando el acceso a sitios catalíticamente activos y causando daño al catalizador en un proceso conocido como coquización. El término de coquización describe la formación de materiales carbonosos que se adhieren a la superficie del catalizador y disminuyen la actividad catalítica.
Conclusiones del estudio
Daeneke afirma que “no podemos ir hacia atrás en el tiempo, pero sí conseguir con el CO2 vuelva a ser carbono y, así, poderlo almacenar”. Una matización importante expuesta en el estudio tras estos resultados se encuentra en la siguiente puntualización; el proceso pueda experimentar una gran evolución y lograr esa conversión. Pero esto no quiere decir que se abra una puerta a seguir contaminando como hasta ahora. Es decir, que se pueda revertir las emisiones de CO2 no es una panacea contra el cambio climático.
Las políticas para mitigarlo deben proseguir para acabar con las emisiones. Si bien su hallazgo puede ayudar a eliminarlo, lo principal, es reducir el consumo de producción industrial y una mayor utilización de energías renovables. Máxime teniendo en cuenta que hablan de una técnica que tardará mucho tiempo en poder usarse de manera completa, a escala total. Por lo que durante ese tiempo se debe seguir luchando contra el cambio climático.








