Carol W. Greider, ‘Nobel’ de Medicina 2009
Carol Widney Greider nace en 1961 en San Diego, California. Desde niña tuvo dificultad con la gramática, y años después descubrieron que era disléxica. Se licencia en biología en 1983 en la Universidad de Santa Bárbara de California, siguiendo sus estudios en biología molecular en la Universidad de Berkeley, siendo alumna de Elizabeth Blackburn. En 1984 identificó la enzima telomerasa, responsable de proteger la integridad de los cromosomas. Un hallazgo que ayudó a poner en marcha un campo de investigación dentro de cuestiones como la longevidad, la biología del cáncer y dentro de la industria de la biotecnología. Con Blackburn, en 1985, descubre la enzima telomerasa, la responsable del mantenimiento cromosómico y formada por telómeros.
Tras terminar la tesis post-doctorado en 1987, Carol Widney Greider prosiguió sus investigaciones en el Laboratorio Cold Spring Harbor en Nueva York. Durante seis años trabajó con el científico Cal Harley, con quien estudió el papel de la telomerasa en el cuerpo humano, descubriendo que se reactiva en las células cancerosas, provocando la aparición de tumores, publicando un estudio en 1990 que ocasionó que Greider fuese promovida a investigadora asistente.
En 1997 Carol Widney Greider se traslada a Maryland y entra como docente en la Escuela de Medicina de la Universidad de Johns Hopkins de Baltimore, donde conseguirá la cátedra de Biología Molecular y Genética. En 2004 fue elegida miembro de la Academia Nacional de Ciencias y ha recibido prestigiosos premios por sus investigaciones como el Premio Albert Lasker (2006), Premio Paul-Ehrlich-und-Ludwing-Darmstaedter (2009) y el Premio Nobel de Medicina (2009), en los tres casos compartidos con Blackburn. Así se convirtió en una de las de las importantes científicas actuales.
¿Qué es la telomerasa?
La telomerasa, también llamada transferasa terminal, es una ribonucleoproteína que agrega una secuencia de repetición de telómeros dependiente de la especie al extremo 3′ de los telómeros. Un telómero es una región de secuencias repetitivas en cada extremo de los cromosomas de la mayoría de los eucariotas. Los telómeros protegen el extremo del cromosoma del daño del ADN o de la fusión con los cromosomas vecinos. La mosca de la fruta Drosophila melanogaster carece de telomerasa, pero usa retrotransposones para mantener los telómeros.
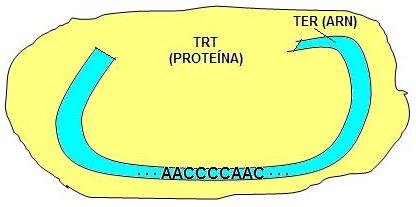
La telomerasa es una enzima transcriptasa inversa que transporta su propia molécula de ARN que se utiliza como plantilla cuando alarga los telómeros. La telomerasa es activa en los gametos y la mayoría de las células cancerosas. Sin embargo normalmente está ausente o en niveles muy bajos en la mayoría de las células somáticas.
Su aplicación contra el cáncer
El mantenimiento de los telómeros a través de la reactivación de la telomerasa es un sello casi universal de las células cancerosas. Esto permite la inmortalidad replicativa. Por el contrario, la actividad de la telomerasa se silencia en la mayoría de las células somáticas adultas. Por tanto, la telomerasa representa un objetivo atractivo para terapias contra el cáncer altamente selectivas.
Sin embargo, el desarrollo de inhibidores de la telomerasa ha sido un desafío. Y es que hasta ahora no existen estrategias clínicamente aprobadas que aprovechen este objetivo del cáncer. El descubrimiento de mutaciones prevalentes en la región promotora de TERT en muchos cánceres y los avances recientes en la biología de la telomerasa ha llevado a un interés renovado en la selección de esta enzima.
Los esfuerzos recientes dirigidos a la telomerasa, incluidas las inmunoterapias y los inhibidores directos de la telomerasa, así como los enfoques emergentes, se han dirigido a la expresión del gen TERT impulsada por mutaciones del promotor TERT.
También se abordan algunos de los desafíos de las terapias dirigidas por telomerasa. Entre ellas esta la posible resistencia terapéutica y las consideraciones para futuras aplicaciones terapéuticas y su traducción al entorno clínico. Aunque queda mucho por hacer, las estrategias efectivas dirigidas a la telomerasa tendrán un impacto transformador para la terapia del cáncer. La perspectiva de fármacos clínicamente efectivos se ve impulsada por los avances recientes en los modelos estructurales de la telomerasa humana.






